- �����������̷���
- ��ѧ���Ӿ�������
- LED/Һ��/��·�徻������
- ʳƷ���Ͼ�������
- ��ױƷ���ջ�����������
- ҽ����е��������
- ҽԺ�����Ҿ�������
- ������ҩ��������
- �ྻʵ���Ҿ�������
- �������Դ��������
- ����/���վ�������
- ���ϻ�����������
- ���/��Ϳ��������
- �ֲ�������ϵͳ����
- �ྻ��/������վ
- ������ˮ��
- ���º�ʪϵͳ
- �ྻ�������豸����
- ���и�Ч����������
- ������/������
- ���ݴ�/�Ծ����ݴ�
- MAC/FFU������
- ��������̨
- ��Ч�����ͷ��
- ���ྻ�ҽྻ��������֪ʶ��ѵ
- �������������ƶ�����
- ���ྻ���价�����������
- ����Ⱦ��ҽԺ������ƹ淶(ȫ��������
- �������ڿ���������������˵��
- ���·������㷽��
- �������������������˵��
- ���ྻ�Ҳ��Լ�¼���ο�
- �������������ྻ���������������
- ���뵼������������ƶ�����
- ��ҽ����е�ྻ�һ����������ƶ�
- ������ױƷ�������������淶��2022���
- �������Ƽ�����GMP��֤Ҫ��
- ����ױƷ�������ɼ�������취�������
- �����ҵȼ���ζ���
- ��ϵ�ˣ�������
- ��ϵ�绰��137-10902965
ҽ����е������ҵ��ο��ƽྻ�ȣ�
ҩ����ڶ�����ҽ����е������ҵ��չGMP�ֳ��˲�ʱ�������Ľྻ�������ص������֮һ��
Ŀǰ�ྻ���������Ҫ������·��漰����
-
��ҽ����е�������������淶��¼��ҽ����е/ֲ����ҽ����е/��������Լ�����
-
��ҽ����е�������������淶��ҽ����е/ֲ����ҽ����е/��������Լ��ֳ����ָ��ԭ��
-
GB 50073-2001���ྻ������ƹ淶��
-
GB 50457-2008��ҽҩ��ҵ�ྻ������ƹ淶��
-
GB/T 16292-2010��ҽҩ��ҵ�ྻ�ң������������ӵIJ��Է�����
-
GB/T 16294-2010��ҽҩ��ҵ�ྻ�ң������������IJ��Է�����
-
YY 0033-2000����ҽ���������������淶��
��Ϊ�ྻ����������
��Ҫ�Գ��������ﺬ�����п��Ƶķ��䣨�����佨���ṹ��װ���������þ����м��ٸ÷��䣨��������ȾԴ�Ľ��롢�����������Ĺ��ܡ�
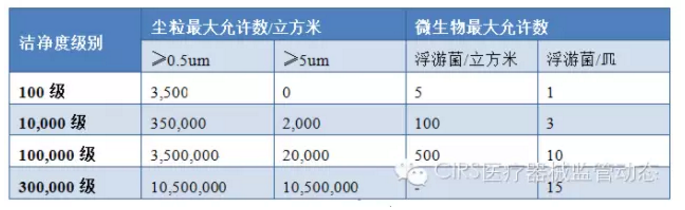
��Ϊ�ྻ�ȣ�
�ྻ�����ڵ�λ��������ں��д��ڻ����ijһ�������������ӵ�����ͳ������
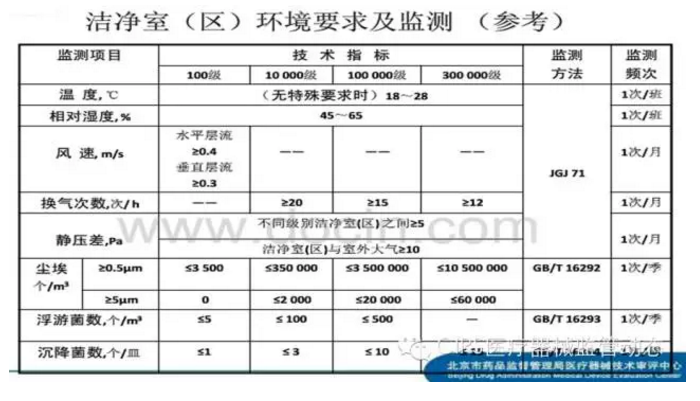
�ྻ�������
�ྻ�ҵĿ��Ʋ�����
-
��������������;
-
�¶Ⱥ����ʪ��;
-
������������ѹ��;
-
����;
-
�·���;
-
�Ծ�ʱ��
�ྻ�ȼ�������ԭ��
|
��Ʒ |
�ྻ�ȼ��� |
|
ֲ��ͽ��뵽Ѫ�ܵ���е����Ѫ��֧�� ����ϴ�㲿���ļӹ���ĩ����ϴ����װ������װ�����ڣ��� |
������10��000�� |
|
ֲ�뵽������֯����е�����������˹��ؽ� ����ϴ�㲿���ļӹ���ĩ����ϴ����װ������װ�����ڣ��� |
������100,000�� |
|
���������˱����ճĤ�Ӵ�����е����������ϵ� ����ϴ�㲿���ļӹ���ĩ����ϴ����װ������װ�����ڣ��� |
������300,000�� |
|
����Ҫ��������������ӹ��ģ���Ѫ��֧��Ϳҩ |
��10,000���¾ֲ�100���ྻ���� |
|
ע�� �������װ���ϲ�����еֱ����Ӵ��������ڲ�����300,000���°�װ�� �ྻ��������ϴ������ʹ��ྻ�������ҡ�ר�ù�λ���ߵ�ĩ����ϴ������������Ŀ����ྻ�ȼ���ɵ���������һ������ |
|
Ӱ��ҽҩ��ҵ�ྻ�ҽྻ�ȵ�����˵��
������ྻ�Ȳ��ϸ��ԭ�Ľ���ʩ
�����ͽྻ�ҵĽྻ�������úͷ�����ο�
�����ྻ�ȼ�ⳣ������˵��
������ྻ����α��֣�
��һ������ν���ҽ����е�ྻ��������֤��ȷ�ϣ���һ����ҽ����е�ྻ��ע��Ҫ�㼰���ܳ��ֵ�����������
��������
���ڡ���ɽ����ݸ����ɽ�����š����ݡ����ݾ������̹�˾|������|�ྻ��|����|��������|��������|�ྻ����|�ྻ����|�ྻ��|GMP����|GMP�����ȿյ��ྻ����ʩ��������
��չ�Ķ���10���������|ʵ�鶯�﷿|�������|�ྻ�һ�������|�ྻ�����ҹ淶|GMP�ྻ�ȵȼ�|ʳƷ���������淶|�ྻ����ʩ��Ҫ��|��������װ�淶
Copyright © 2012-2018


